El Instituto de Salud Pública (ISP) suspendió la distribución y comercialización en Chile de todos los medicamentos que contengan nimesulida, un antiinflamatorio de uso común en el país, por el riesgo de contraer una enfermedad en el hígado asociada al consumo de este medicamento.
Lo anterior, tras un informe realizado por la Red de Centros de Información de Medicamentos de Latinoamérica y el Caribe (RedCIMLAC), del cual el ISP forma parte a través de la sección información de medicamentos.
Este informe se basó en una revisión de estudios clínicos, que comparaban el uso de nimesulina con otros antiinflamatorios, en los que se mostró la existencia de mayor riesgo de daño en el hígado a causa de nimesulida, documentándose 75 casos de pacientes con daño hepático por causa de este fármaco, 10 de los cuales terminaron en muerte en Latinoamérica.
“El daño hepático provocado por la nimesulida no depende de la dosis administrada, es decir, es una reacción inusual que depende de la respuesta del paciente al medicamento y, por ello, es considerado un daño difícilmente predecible”, señaló David Mena, químico farmacéutico del Subdepartamento de Farmacovigilancia.
En concreto, la nimesulida es un antiinflamatorio analgésico utilizado en el tratamiento de inflamaciones y control de dolor. El consumo de nimesulida en nuestro país, desde 2012 a 2016, fue aumentando hasta las 475.000 unidades de venta.
En el Centro Nacional de Farmacovigilancia del ISP se han reportado siete sospechas de reacciones adversas de medicamentos relacionadas con problemas hepáticos asociados a este fármaco, de las cuales seis han sido consideradas serias. Al igual que países europeos como España, Francia y Finlandia, la autoridad sanitaria decidió el retiro total de estos fármacos debido a los antecedentes y la disponibilidad de otros antiinflamatorios como alternativa terapéutica.
El ISP recomienda a los pacientes que actualmente están bajo tratamiento con el medicamento nimesulida que se acerquen a su médico tratante para que les proporcione un antiinflamatorio de reemplazo.
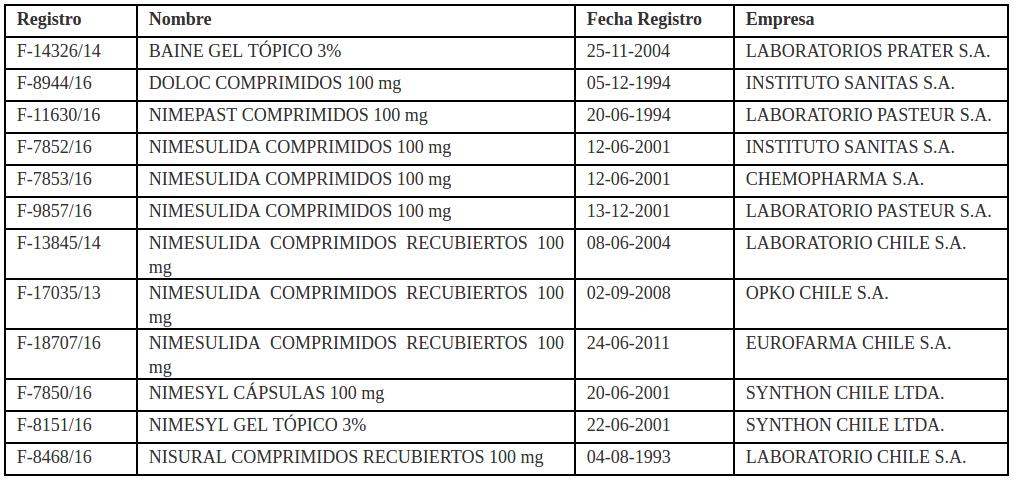
Los titulares de registro sanitarios de productos farmacéuticos que en cuya formulación esté contenida nimesulida deberán informar al ISP, mediante notificación al Subdepartamento de Fiscalización -en un plazo de 20 días hábiles- todas las series o lotes disponibles en sus bodegas y de los retirados a sus distribuidores.
Entre ellos se encuentran unidades elaboradas por los laboratorios Chile, Pasteur, Prater, Instituto Sanitas, Chemopharma, Opko Chile, Eurofarma y Synthon.







 Enviando corrección, espere un momento...
Enviando corrección, espere un momento...